在肿瘤免疫细胞疗法中,γδ-T细胞疗法虽然“小众”,但具有巨大的应用前景。
这是因为,γδ-T细胞作为T细胞的一种非常见亚群,尽管只占人外周血T淋巴细胞的2%-10%左右,但凭借其功能强大且全面的优势,γδ-T细胞疗法正在兴起。目前,已经有不少临床试验使用γδ-T细胞治疗癌症,包括血液恶性肿瘤、头颈癌、肝癌、肾癌、乳腺癌、前列腺癌、神经母细胞瘤和肺癌等。

香港大学涂文伟教授
香港大学涂文伟教授从事免疫研究超过20年,专注于γδ-T细胞及其外泌体的肿瘤免疫治疗和疫苗开发。如今,他正带着多个“全球首发”成果进行科研转化,并希望通过成立公司让技术落地、惠及患者。
在这个过程中,我们看到涂教授及其团队扎实的基础研究功底和具有商业化潜力的技术,但同时也看到了他们所面临的创业挑战。
始于偶然,探索γδ-T细胞淋巴瘤与实体瘤治疗
涂文伟和γδ-T细胞疗法的故事源于偶然。
实际上,在研究γδ-T细胞之前,涂文伟一直关注人外周血淋巴细胞中在数量上占绝对优势的T细胞——αβ-T细胞。涂文伟回忆,2000年,在一次分析心脏移植效应时,偶然发现除了αβ-T细胞外,还存在另外一群T细胞,这引起了他极大的兴趣。
回到香港之后,涂文伟立即鉴定并确认这“一群细胞”是γδ-T细胞。“从那时开始,我就做了大量的工作,来了解γδ—T细胞,关于γδ—T细胞怎么抗病毒?怎么在体内作用?”
此后,涂文伟便以“γδ-T细胞疗法”为明确的方向,进一步开展系统研究,并在实验室中构建起人源化小鼠模型,来验证人γδ-T细胞在体内的功效。
“在20多年前,教科书和科研人员都很少提及γδ-T细胞,近几年,γδ-T细胞才被很多科研人员关注并进行研究。”涂文伟表示,尽管沉寂多年,γδ-T细胞依然与众不同,其强大的抗感染抗肿瘤特性使其具有广阔的应用前景。
与传统的αβ—T细胞不同,γδ-T细胞可以在不受MHC限制的情况下识别靶细胞,从而几乎没有移植物抗宿主病(GVHD)。“在临床上,我们可以用第三方正常人的γδ-T细胞对病人进行输入治疗。”涂文伟向橙果局介绍到,这是优质的即用型异体细胞产品。
另外,γδ-T细胞兼具T细胞、NK细胞和抗原呈递细胞的特征,尤其具有强大的细胞毒性,使其能在2h左右对肿瘤细胞进行杀伤。
随着对γδ-T细胞疗法的深入与理解,2014年,涂文伟团队首次证明,帕米磷酸钠可以通过靶向性激活人类Vγ9Vδ2-T细胞,来控制EB相关性疾病,包括B细胞淋巴瘤及移植后淋巴细胞增生性疾病。
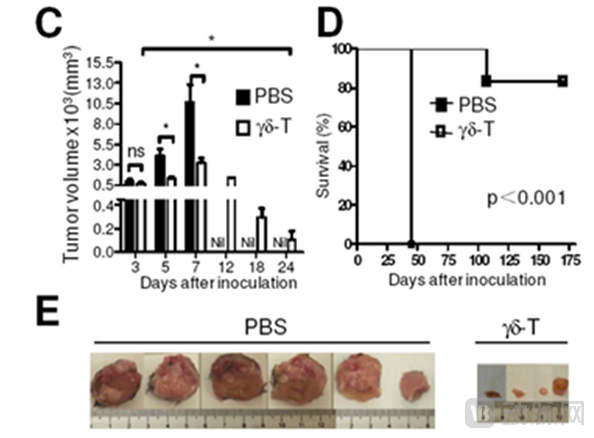
“我们用γδ-T细胞治疗淋巴瘤有很好的治疗效果,在实验中,对照组小鼠在50天左右全部死亡,而输入γδ-T细胞的治疗组小鼠,有80%左右的存活期达到175天。”涂文伟向橙果局透露,目前,这一发现正在开展临床研究。

之后,又在2021年,团队与暨南大学尹芝南教授合作,在全球率先完成了同种异体γδ-T细胞治疗晚期肝癌、肺癌等实体瘤床的临床研究。据悉,肝癌组未治疗患者的中位生存时间为8.1个月;相比之下,接受γδ-T细胞治疗的患者的中位生存时间为23.1个月。在肺癌组,未治疗患者的中位生存时间为9.1个月;接受γδ-T细胞治疗的患者的中位生存时间为19.1个月。
在γδ-T细胞外泌体研究中做到first in class
尽管依据自身的天然优势,γδ-T细胞在异体治疗、实体瘤治疗上具备极大潜力,但它仍面临的许多阻碍。
比如γδ-T细胞杀伤肿瘤的活性被肿瘤微环境抑制而导致疗效不稳定、在某些癌症患者中γδ-T细胞难以完成体外扩增、在某些肿瘤的微环境下可能诱导γδ-T细胞变为促进肿瘤生长等。
因此,涂文伟及其团队进一步探寻基于外泌体的无细胞疗法。
所谓外泌体,即是胞内体起源的细胞外小囊泡,与母细胞的成分相似,介导细胞间的通讯。与基于细胞的疗法相比,无细胞的外泌体有更高的安全性、更低的成本和更好的抗肿瘤活性。
通过大量研究,涂文伟团队发现γδ-T细胞外泌体携带诱导死亡的配体(FasL和TRAIL)和免疫刺激分子(CD80、CD86、I类和II类MHC),这不仅能通过FasL和TRAIL途径有效杀死肿瘤细胞,还能促进肿瘤抗原特异性CD4和CD8T细胞扩增。
同时,涂文伟团队还发现,同种异体γδ-T细胞外泌体在人源化小鼠中比自体γδ-T细胞外泌体更有效的抗肿瘤活性。这是因为,同种异体γδ-T细胞外泌体增加了T细胞向肿瘤组织的浸润,并诱导了更强大的CD4和CD8 T细胞介导的抗肿瘤免疫力。
换句话来说,与具有直接细胞毒性抗肿瘤活性的NK细胞或树突细胞衍生的外泌体相比,γδ-T细胞外泌体具有直接杀死肿瘤细胞并间接诱导T细胞介导的双重抗肿瘤活性,从而更有效地抑制肿瘤。

团队最新的研究进一步表明,γδ-T细胞外泌体可联合放疗达到更好的治疗鼻咽癌效应。同时,首次证明,γδ-T细胞外泌体抗肿瘤效应不受免疫抑制性的肿瘤微环境影响。

涂文伟向橙果局说道:“针对γδ-T细胞外泌体研究,我们是全世界第一个有成果的,也是第一个发表相关文章的团队。在未来一两个月,我们也将会发表全球第一篇关于人的γδ-T细胞外泌体的肿瘤疫苗的文章。”
临床研究与商业化同步推进
谈及科研成果转化,涂文伟表示,“最好能成立公司,一边进行临床研究,一边推进商业化。”
而从科学家转变为创业者并不是一件容易的事。涂文伟坦言,“虽然团队在临床研究上累积了丰富的经验,但对于如何经营公司,我们完全是‘门外汉’。”
这也正是当下科研成果所面临的普遍困难,科学家们将最前沿的研究成果带到了产业中来,让创新能力从跟随创新向着原研发力。
但不可否认的是,当科学家走出实验室进行企业管理时常常力不从心。在实验台前游刃有余的他们,在面对技术的产业化时也会感到困惑。他们意识到科研创新并非技术和产品创新的全部。在科研创新以外,他们需要引进新的力量,引进产业和商业化视野。
因此,在科学家创立的企业中,“科学家+创业合伙人/CEO”的团队组合成为一种流行公式。对此,涂文伟教授也做了相应的规划。当前,他正在积极培养和寻找商业化人才,帮助团队一起创建技术平台型公司。此外,选择投资人时,涂文伟教授也更加倾向于具有孵化明星企业经验的实力派投资机构,这样更能够为团队提供更加合理的商业化路径。
“目前,项目已经走出纯粹的实验室阶段,并达到临床试验的标准,计划在3年内完成I期临床,在5年内完成II、III期临床。”涂文伟表示,团队接下来将会重点关注临床试验和规模化生产两方面工作,并与各方伙伴及投资人搭建起良好的合作关系。