在人们以为新冠疫情已经过去的时候,新的突变株XBB.1.16再次来袭,过去一个月(2023.3.20-2023.4.16),全球仍有280万确诊病例和1.8万人死亡。
实际上,人类对病毒的认识直接关系到人类自身的生活与健康,尤其是新型冠状病毒肺炎(COVID-19)在全球范围内呈大流行趋势,基于其致病病原体新型冠状病毒(SARS-CoV-2)的新冠疫苗研发工作成为一大热点。
早在博士时期,武汉大学病毒学国家重点实验室PI徐可教授就开始关注流感病毒的广谱疫苗研究。经过20年的技术革新与沉淀,2023年1月,她领导团队再次为广谱疫苗研究领域带来新的成果——在Science Translational Medicine发表了研究论文“Vaccination with Span, an antigen guided by SARS-CoV-2 S protein evolution, protects against challenge with viral variants in mice”,并提出了应对新冠病毒不断变异的广谱疫苗设计新策略。

先要理清病毒进化方向,才能跑赢病毒变异速度
随着病毒传播与流行的时间越长,病毒不断迭代变异,再加上人体免疫以及疫苗免疫的选择压力,新冠病毒已由最初的原始毒株进化出多谱系的变异毒株。
目前,世界卫生组织将流行的重要变异病毒命名为重点关注变异株(VOC),其中包括Alpha、Beta、Gamma、Delta 和 Omicron五个大类。
“尽管变异体的进展似乎在很大程度上是不可预测的,但病毒进化显然存在一些潜在的趋势。”徐可表示。在对一千一百多万个新冠病毒序列进行了全面研究后,团队首次发现在人群中存活下来的病毒分离株中,新冠病毒刺突蛋白(以下简称为S蛋白)的突变并不是随机的,而是沿着三条定向路径进化。
第一条路径是以Delta株和Lambda株为代表的“高细胞感染性+弱免疫逃逸能力”,第二条路径是以Gamma株为代表的“低细胞感染性+强免疫逃逸能力”,而第三条路径则是以Beta株为代表的“高细胞感染性+强免疫逃逸”,但变异株数量相对较少。
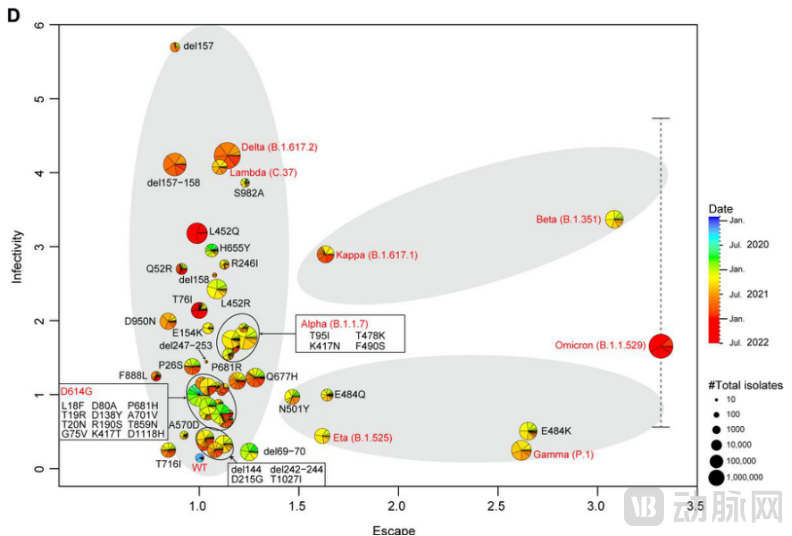 新冠病毒S蛋白的进化规律
新冠病毒S蛋白的进化规律
S蛋白进化成高感染性加低免疫耐药性或低感染性加高免疫耐药性的不同进化路径,定向进化的突变导致抗原性的异质化。这也是目前的单一毒株疫苗只能为一组变异株提供窄谱保护,而不能为其他变异株提供宽谱保护的重要原因。
“病毒进化的规律告诉我们,如果我们一叶障目,选择单一方向去追逐病毒会让另一个进化方向的病毒漏网,直接导致疫苗失效。所以,我们需要再用一种全新的方式去预测病毒进化的轨迹,才最有可能跑赢病毒变异的速度。”徐可表示。
基于病毒进化共识序列,设计人工抗原Span
如何让疫苗研发跑在病毒变异前面?
对此,徐可团队首次提出将流感病毒的通用疫苗策略——通过共识序列的保守表位“创造法”进行新冠疫苗研发。
谈及原因,徐可说:“我从2003年开始,就关注流感广谱疫苗。流感与新冠肺炎同属于呼吸道疾病,在新冠肺炎刚爆发不久,我们发现它们的模式有很大的相似之处。因此,也意识到这两个病毒很可能是互相纠缠的。”
为了进一步验证这一猜想,徐可团队让实验小鼠同时感染流感和新冠,发现实验小鼠肺部感染的病理表现越来越强。这说明两个病毒可以发生叠加和共感染的情况。
这一实验结果提示了流感、新冠双价疫苗的必要性,并将成果发表在亚太地区影响力最高的科学杂志《Cell Research》上。这也更加明确了团队的研究方向——由于两个病毒具有类似特性,团队之前开发的基于病毒进化共识序列的流感疫苗设计策略,在新冠病毒中也很可能适用。
所谓病毒进化共识序列,是基于进化计算的共性突变位点跟踪。它去除了人为选择的偏好性,再公平的、全覆盖的寻找在病毒变异种群中保留下来的共性变异。
“这些共性的变异会在亲本病毒和子代病毒中同时留下,代表着病毒适应宿主的多种进化方向的最大集合,因此,这类变异对于病毒来说是比较保守的,也是倾向于一些更稳定、更优化的功能。”徐可解释到。
团队得到病毒进化共识序列,是一个寻找的过程,也是一个计算的过程。据了解,徐可团队先从数据库中下载2675条新冠病毒S蛋白氨基酸序列,并再经过进化分类和计算,才最终设计了一种覆盖共性突变的拟合新抗原(Span)。
其中,团队采用的计算方法是进化聚类,对序列的每个时间轴和进化距离进行聚类。当数据的聚类结构发生了显著的变化,团队成员则必须调整算法以反映新的结构。
在做完大量计算统计工作后,徐可团队筛选出五个不同进化枝的最常见突变,包括D614G、del69-70、del144、N501Y 和 P681H,并研究计算所有突变位点的发生频率。最后在重建的系统发育树中,Span序列位于系统发育树的中心,表明其共识特征。
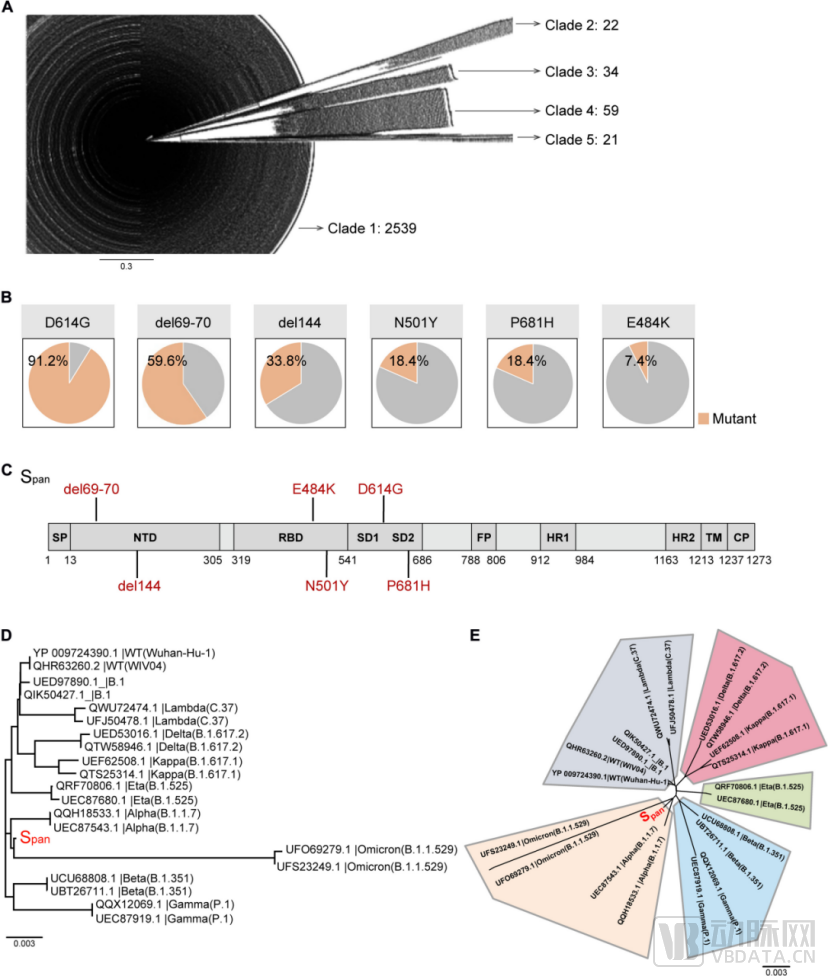 SARS-CoV-2 S蛋白进化用于指导S蛋白的设计泛序列
SARS-CoV-2 S蛋白进化用于指导S蛋白的设计泛序列
“无论新冠病毒在人群中如何变异,它们都来自相同的祖先并向着更加适应宿主的方向进化,而这个进化方向一定是有序的,而不是杂乱无章的。因此,理想的广谱疫苗抗原应在保留祖先病毒印记的同时包含代表进化方向的大多数变异株的共识位点,以促进这些变异株和其他变异株的广泛中和。”徐可说到。
不仅如此,新抗原Span还具有极强的预见性。这是因为未来的病毒也会携带共性位点。值得关注的是,在Delta出现之前(2021年2月),已经完成设计的Span,却能高效诱导针对设计后出现的Delta和Omicron及其变异株的广谱中和抗体。
要证明Span是否真的可以作为针对异质变体的广谱疫苗抗原,实验还是唯一的检验标准。
因此,徐可团队展开两个小鼠实验,不仅评估了Span疫苗能保护小鼠免受WT、Beta 和 Delta SARS-CoV-2伤害,还证明了接种过 Span疫苗加强针的小鼠对奥密克戎变体的致死感染具有完全保护。
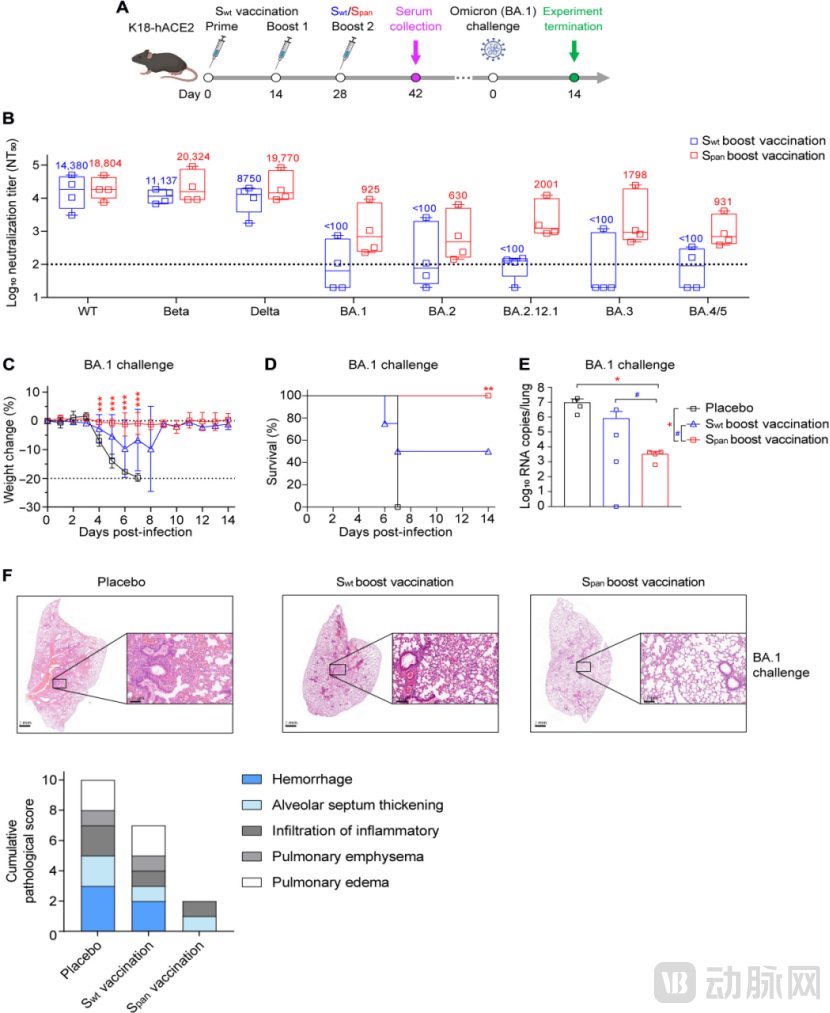 Span加强疫苗接种可保护小鼠免受奥密克戎变体实验
Span加强疫苗接种可保护小鼠免受奥密克戎变体实验
解决未来变异的研发,面向未来需求的转化
让成果走出实验室。
当前,这一创新的新冠广谱疫苗设计构想已经完成概念性验证。而徐可团队也期待他们的成果能为社会带来更多的价值。
一方面是满足极大的市场需求,面对全人群易感而又不断变异病毒,广谱疫苗是必然的未来。在徐可看来,倘若新冠广谱疫苗能够实现产业化,将有望在世界范围内实现流通,并获得不可预估的市场份额。从理论而言,广谱疫苗可以作用于全人类,比如接种率仅有10%的国内市场就是等待开发的蓝海,而对于接种过的群体也可以当成加强针使用。
另一方面是基于病毒进化共识序列这一底层技术,团队还将成立创新公司,布局多个管线。据介绍,该技术突破了现有广谱疫苗的内部抗原、茎干区、以及马赛克嵌合等方法的有限广谱范围的限制,是基于抗原进化规律的序列优化,是全新的广谱疫苗顶层设计理论。因此,它也被认为是最可能具有预见性、覆盖未来突变的技术方案。
“不仅是当下流行的新冠病毒,我们能够迅速跟上市场需求,成为全球首支用广谱疫苗预防新冠肺炎的研究团队。另外,我们还关注急需广谱疫苗的其他的呼吸道疾病,以及像手足口病这类疫苗效果不佳的方向。”徐可说到。
当然,要在转化这条路上行稳致远,离不开内在的修炼。
在徐可的带领下,团队已经累积20年的研究经验,不仅在Science Translational Medicine、Vaccine等多个国际期刊发表研究论文,还申请了《新型冠状病毒突变株S蛋白及其亚单位疫苗》的发明专利,用理论科学和实验科学指导疫苗设计。
 徐可教授(左二)及其团队成员,受访者供图
徐可教授(左二)及其团队成员,受访者供图
据了解,目前团队规模达到23人,其中有一半以上的成员专注于广谱疫苗的应用研究,正在进一步推动系列创新疫苗的转化落地。
附徐可教授课题组招聘
(一)CMC药物制剂部门总监 1名
1、熟悉蛋白制品的表达纯化和批量生产的流程,熟悉IND申报资料标准,具有疫苗研发经验者优先。
(二)博士后 1名
1、年龄35岁以下,获得病毒学相关博士学位不超过3年或即将获博士学位,以第一作者在SCI期刊至少发表过一篇高水平的研究型论文;
2、 具有病毒学、免疫学、微生物学等相关专业背景,熟悉常规病毒学、细胞生物学、生物化学的实验技术,具有小动物研究经验和生物安全实验室从业经验;
3、具有独立负责和开展科研项目的能力,积极申报各类博士后和国家基金;具有较高的英文表达及写作水平,能独立撰写和发表SCI论文;
4、团队合作意识强,拥有认真负责的工作态度、积极创新的科研热情。
*工作地址:湖北省武汉市武昌区八一路武汉大学生命科学学院/病毒学国家重点实验室
应聘方式:应聘者请将个人简历、3篇代表性论文、推荐信等相关材料,整理为一个PDF文档发送至周老师,邮箱:zhouchanjuan@whu.edu.cn,邮件请注明“应聘博士后+姓名+学校”,简历命名方式请与邮件标题保持一致,如有其他疑问也可致电:027-68753227。应聘者材料将严格保密。