说起时下最热门的生物医药话题,GLP-1减肥药称第一,大概只有阿尔兹海默病可以数第二。
8月末,国内的中成药企业通化金马,宣布完成了琥珀八氢氨吖啶片III期临床试验盲态数据审核,用于治疗阿尔兹海默病。这是继绿谷制药的甘露特钠胶囊后,国内进展最快的阿尔兹海默病新药。消息一出,二级市场一片欢腾。在此后的交易日中,通化金马的股价8次冲上涨停板。
与此同时,阿尔兹海默病的早诊早筛,成为临床检测企业新的发力点。过去数月间,丹纳赫、热景生物等国内外企业,纷纷扎进阿尔兹海默病检测赛道,裹挟着大量资金、创新团队加入,让阿尔兹海默病的早诊早筛,成为2023年生物科技领域中最热闹的风景。
阿尔兹海默病的诊疗变局,正悄然发生。
治疗阿尔兹海默病,一直是全世界跨国药企奋力想要攻下的堡垒,这是一座富矿。
据阿尔茨海默病协会在2021年的一份研究测算,全球每年新增阿尔兹海默病患者350万人。在国内,根据第7次全国人口普查数据,到2020年11月1日,我国60岁及以上老年人口数达到2.6402亿人,另一个统计数据显示,2020年,国内60岁及以上的阿尔兹海默病患者约983 万人,大约每27个60岁以上的老年人中,就有一人患有阿尔兹海默病。
在过去,有长达30年时间,全球没有一款阿尔兹海默病新药获批上市。数据显示,2000年至2017年间,全球研发失败的阿尔茨海默病临床药物超过300种,失败率高达99.6%。渤健、诺华、礼来等大药企花费数百亿美元,反复折戟于此。2023年3月,礼来放弃了研发20多年的Solanezumab,原因是仍没有足够的临床证据表明,Solanezumab可以清除或阻止Aβ蛋白斑块积聚,减缓阿尔茨海默病早期患者的认知能力下降。而在1年前的11月14日,罗氏也宣布其在研的阿尔茨海默病药物Gantenerumab III期临床研究失败。
转折出现在2020年前后。2019年,国产的甘露特钠胶囊获批上市,阿尔兹海默病特效药开启商业化进程。目前为之,全球已经有3款可以有效减缓阿尔兹海默病患者病程的新药。不过,现有的临床数据表明,这些阿尔兹海默病新药的有效性和安全性,主要针对早期患者。
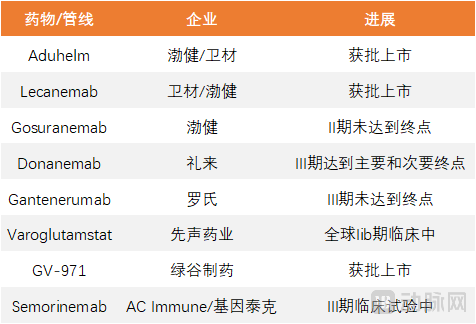
部分阿尔兹海默病特效药研发进展 数据来源:动脉橙数据库
2021年6月,渤健开发的β淀粉样蛋白抗体Aduhelm获批上市,用于治疗早期阿尔兹海默病患者。这是自2003年以来,FDA批准的首个用于治疗阿尔兹海默病的新药。
上市以来,关于Aduhelm的有效性和安全性,一直存在争议。获批之初,FDA就要求渤健进行第4阶段的研究,来确认药物获益。Aduhelm的商业化表现并不亮眼。渤健的2022年财报数据显示,Aduhelm创造的收入为480万美元,相比上年增长60%,是渤健产品管线中相当乏善可陈的存在。
Aduhelm不算成功的商业化表现,并没有让跨国药企对阿尔兹海默病新药的商业化失去兴趣。到2023年,阿尔兹海默病新药的市场逐渐热闹。
7月6日,卫材和渤健研发的阿尔茨海默病治疗药物Leqembi获得FDA的批准上市。这次,FDA没有要求卫材和渤健在上市再做临床研究,对Leqembi的安全性和有效性高度认可。不过,Leqembi针对的,仍然是早期的阿尔兹海默病患者。
仅仅10多天后,礼来也宣布,已经向FDA提交了阿尔茨海默病新药Donanemab的上市申请,FDA预计2023年年底前做出决定。同样,Dnnanemab所针对的,也是阿尔兹海默病的早期患者。
此前的2023年5月,礼来公布的数据显示,Donanemab在18个月内将某些早期阿尔茨海默病患者的认知和功能下降速度减缓了35%。而Leqembi 的3期关键临床试验数据显示,它在18个月内使阿尔茨海默病患者的认知和功能下降速度减缓了27%。Leqembi每两周给药一次,Donanemab每四周给药一次。外界纷纷推测,如果Donanemab获批上市,将对卫材和渤健刚刚攻下的阿尔兹海默病市场形成冲击。
在Leqembi的上市前研究中,还对早期阿尔兹海默病患者做出了明确定义,即出现轻度认知障碍或轻度痴呆,且已被证实大脑中存在淀粉样斑块的患者,而晚期阿尔茨海默病患者则可能无法从Leqembi中受益,甚至可能面临更大的安全风险。
在这样的背景下,如何把早期阿尔兹海默病患者找出来,成了新的问题,阿尔兹海默病早诊早筛市场随之热闹起来。
传统上,阿尔兹海默病并不存在早诊早筛这件事。在阿尔兹海默病无药可用的时期,早诊早筛没有临床价值。客观上,常规的诊断工具也无法筛查出早期的阿尔兹海默病患者。
所以当前大火的阿尔兹海默病早筛市场,其实是摸着石头过河。
一方面,阿尔兹海默病早诊早筛领域迎来了全球龙头的重磅加持。2023年7月,全球IVD巨头丹纳赫旗下的贝克曼库尔特公司宣布,将与日本医学检测老牌龙头Fujirebio合作,共同开发用于阿尔茨海默病和其他神经退行性疾病的新生物标记物。在此之前,跨国巨头在阿尔兹海默病之上的关键布局,都集中在治疗环节。全球巨头在阿尔兹海默病之上落下的首子,即在早诊早筛场景。
此番丹纳赫与Fujirebio合作,最主要的目的是尝试用血液取代脑脊液,来筛查阿尔兹海默病筛查。此举对于阿尔兹海默病早诊早筛而言,此举意义重大。临床上,阿尔兹海默病的确诊手段,除了简单的精神量表外,神经影像学检查和脑脊液CSF检查,通常被用来诊断阿尔兹海默。
具体而言,神经影像学检查,主要通过头部CT和MRI检查,来发现脑皮质萎缩,对于早期的阿尔兹海默病很难检出。脑脊液检查可以直接反映脑组织的病理改变,能先于医学影像,发现阿尔兹海默病。但脑脊液检查取样过程带来的创伤,让许多人难以接受。
在神经退行性疾病的生物标记物开发方面,Fujirebio一直走在世界前列,已经建立了丰富的生物标记物体系。2022年,Fujirebio开发的基于脑脊液的Gβ-淀粉样蛋白比率(1-42/1-40)检验,获得了FDA的新分类。在此之前,Gβ-淀粉样蛋白比率(1-42/1-40)已经广泛地被欧美医生用来筛查怀疑地阿尔兹海默病患者。一旦开发初基于血液的Gβ-淀粉样蛋白比率检测方法,无疑将进一步加速这种筛查方式的市场渗透。
另一方面,阿尔兹海默病早诊早筛的全球创新,正在进入高潮。
仅仅在9月,国内阿尔兹海默病早诊早筛领域就实现了多个从0到1的突破。

国内阿尔兹海默病早诊早筛领域部分新突破 数据来源:动脉橙数据库
9月初,永和阳光开发的阿尔茨海默症检测产品β淀粉样蛋白1-42(Aβ1-42)测定试剂盒(磁微粒化学发光法),也获得了医疗器械注册证。这是国内首个用于阿尔兹海默病检测的化学发光试剂盒。
9月15日,先通医药产品欧韦宁®氟[18F]贝他苯注射液获得国家药品监督管理局(NMPA)批准上市。这是国内首个获批用于阿尔兹海默病诊断的Aβ-PET显像剂,可实现早期、精准、无创的AD诊断。据了解,欧韦宁®用于脑正电子发射断层扫描(PET)显像,通过测定脑内β-淀粉样蛋白斑块沉积水平,进行阿尔茨海默病(AD)的诊断、鉴别诊断和疗效评估。
到了9月末,由医未(铱硙)医疗研发的全球首款专注于阿尔茨海默病(AD)磁共振影像辅助评估软件——医未脑医生,正式获批NMPA三类医疗器械注册证。这是全球首款获批的应用于AD诊疗辅助评估的人工智能(AI)软件产品,也是中国第一张AD软件三类证。在此前的临床验证中,医未脑医生独立诊断的灵敏度、特异度均突破90%,相比一般医生诊断水平有非常大优势。
此外,豪思生物自主研发了阿尔茨海默症早期独家检测产品,能够在临床症状出现前检出AD并准确分期,根据分期及时制定个体化治疗方案,并通过实时监测,对方案进行精确调整;岚煜生物的老年痴呆检测三项(Aβ1-42/p-Tau-181/AD7c-NTP),作为一种无创性的检查,为AD的早期诊断、早期干预提供重要的时间窗口。各种创新力量的加入,无疑将推动阿尔兹海默病早诊早筛生态的快速成熟。
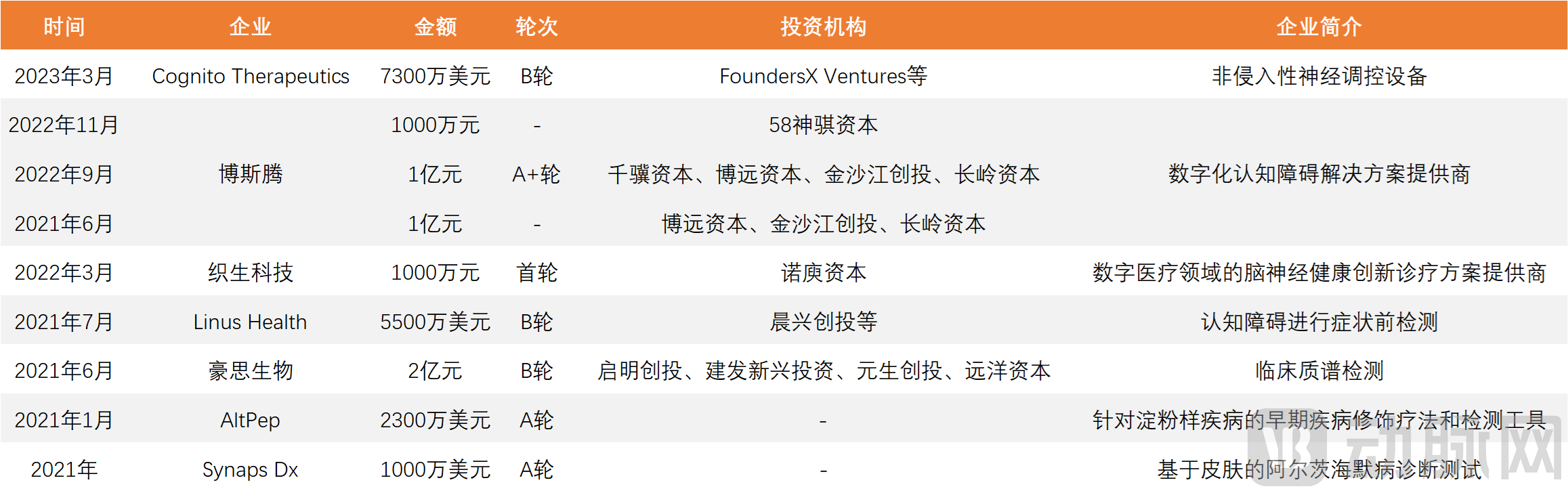 2021年以来全球阿尔兹海默病早诊早筛领域部分融资事件 数据来源:动脉橙数据库
2021年以来全球阿尔兹海默病早诊早筛领域部分融资事件 数据来源:动脉橙数据库
与此同时,2021年以来,以阿尔兹海默病早诊早筛未特色的创新企业频频获得资本关注。据动脉网不完全统计,有近10家相关企业在过去2年间完成了融资,部分企业连续完成多轮融资,启明创投、国科嘉和、金沙江创投等专业机构纷纷入局。
不可否认,至少在商业化的舞台上,阿尔兹海默病正在成为精准诊疗开发者竞逐的下一个场景。
与所有可以通过早筛来获益的疾病类似,作为一种神经退行性疾病,阿尔兹海默病进展缓慢。从大脑中的相关生物标记物出现异常,到患者表现出明显的认知障碍,往往需要10年以上时间。对于阿尔兹海默病而言,通常所讲的早期阶段,是指患者开始出现轻度认知障碍,或者更早的时期。
这个时期的阿尔兹海默病,通过临床症状或者医学影像,都很难判断,患生物标志物指标的异常表现也很细微,不容易检出。从某种意义上讲,阿尔兹海默病的早诊早筛,才刚刚起步,后续还有无数的里程碑需要去攻克。
首先,阿尔兹海默病早诊早筛的数据积累还相对有限,需要持续的临床验证。在现有条件下,还没有任何临床证据表明,单一筛查手段都还不足以用来评估阿尔兹海默病。尽管生物标志物检测在AD早期诊断中意义重大,由于人类对于阿尔兹海默病发生、发展机制研究还不够成熟,关于怎样的生物标记物可以用来独立判断早期的阿尔兹海默病,仍在探索之中。
目前比较一致的观点是,血液Aβ和磷酸化tau蛋白,作为阿尔兹海默病相关血液生物标记物,颇具应用潜力。其中,Aβ1-42、p-tau-181是目前认可度最高、研究最多的两大指标,血液Aβ1-42或Aβ1-42/1-40值、p-tau可用于预测脑内Aβ病理改变和阿尔兹海默病转化率。在2023年的阿尔茨海默病协会国际会议(AAIC)上,美国国家老龄化研究所和阿尔茨海默病协会(NIA-AA)公布了阿尔茨海默病最新诊断标准指南,明确将人β淀粉样蛋白1-42、人磷酸化tau181蛋白血浆生物标志物纳入生物标志物分类、疾病诊断和分期更新标准。
不过,这份诊断标准指南明确,生物标志物应该在临床背景下解释,而不是单独使用,并且在当前可用的技术和证据下,无法确定个体认知缺陷中有多少归因于阿尔茨海默病以及其他神经病理学。此外,有相关指南指出,神经纤维损伤、功能障碍、炎症等不特异于阿尔茨海默病的标志物,对于这种疾病的发生发展,也有重要影响。
其次,即便是采用了指南中明确的生物标志物,阿尔兹海默病早诊早筛也还需要在技术和产品层面进一步优化。比如,目前已有多项研究,开始联合应用外周血蛋白、脂质和代谢物等,包括Aβ42二聚体含量、可抑制Aβ纤维化、解聚Aβ纤维的血浆凝溶胶蛋白(GSN)和GSN主要降解酶MMP3等。不过,由于外周血中,这些生物标志物的含量很低,现有的检测手段,能否在可控的成本范围能精准到足够低的阈值,而检测结果是否能够真正代表中枢神经系统的器质性改变,都还有待进一步研究。
所以,尽管阿尔兹海默病早诊早筛的产品开发和创新投资,正方兴未艾,但在实践中,阿尔兹海默病的主要诊断方法仍是联合诊断,即对于可能的阿尔兹海默病患者,一般要先做认知功能评估,同时配合CT、MRI等影像学检查,来进一步确诊。如果这一套检测下来仍不能确定,则需要使用PET或脑脊液/血液生物标志物检测,获取更多的信息来辅助判断,过程相当繁琐。
最后,也是最棘手的一点,关于阿尔兹海默病早诊早筛的市场认知教育和配套体系,还处于相当早期。大多数人对于阿尔兹海默病的知识非常匮乏。在他们的认知中,早期的阿尔兹海默病被当成老糊涂了的常态,而被忽略,从而错过早诊早筛和缓解病情的机会。即便是掌握了一定疾病知识的人,对阿尔兹海默病早诊早筛的认可度也很低。
显然,风口之上的阿尔兹海默病早筛,还有很长的路要走。






























