近日,四川大学魏于全院士团队公开了一项关于mRNA递送的专利,该专利引入了一种新型递送载体——TLSV纳米粒。这种纳米粒是由DOTAP阳离子磷脂与两亲性双嵌段共聚物mPEG‑PCL精心包裹肿瘤细胞裂解物制备而成,具有低细胞毒性和高转染率等显著优势。
专利中表示TLSV纳米粒与mRNA结合形成的复合物在体内实验中成功抑制了结肠癌肿瘤组织的生长,并展现出预防结直肠癌肺转移的有效效果,这为结直肠癌的治疗提供了新的策略。
已上市19款药物,适应症不断拓展
小核酸药物是一种全新的药物类别,由核苷酸组成,主要作用于细胞质的mRNA,通过碱基互补识别和抑制靶mRNA,实现对蛋白表达的调控,达到治疗疾病的目的。
经过几十年的基础研究,全球共累计有19款小核酸药物上市,这些药物主要用于治疗杜兴氏肌肉萎缩症、脊髓性肌肉萎缩症、遗传性转甲状腺素淀粉样变性等遗传性和罕见疾病。这是因为罕见病具有突破疗法认证、临床试验入组病人数量要求较少、优先评审等优势,有助于企业较快验证其临床效果并上市销售。
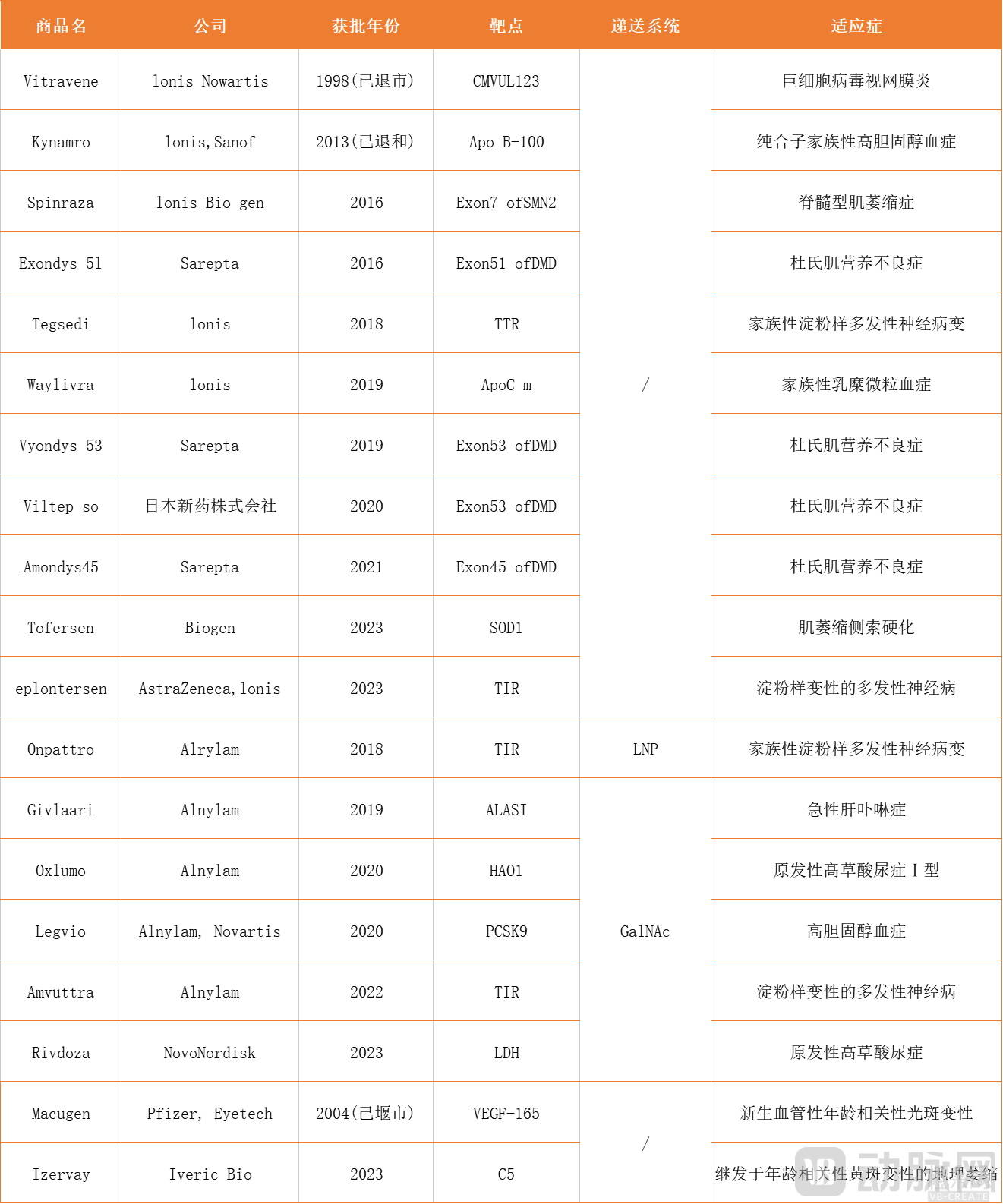 图为19款已上市小核酸药物详情,来源:广州罕见病基因治疗联盟
图为19款已上市小核酸药物详情,来源:广州罕见病基因治疗联盟
而随着小核酸药物研发热情上涨,覆盖靶点增加,其适应症也趋向多样。2020年,诺华的长效降脂药Inclisiran作为全球首个非罕见病领域获批的小核酸药物上市,并在2022年创下1.12亿美元的销售额。
Inclisiran的成功激励着更多企业切入小核酸赛道,拓宽罕见病、心血管代谢疾病的药物版图。比如,信达生物与圣因生物宣布小核酸(siRNA)候选药物SGB-3908用于治疗高血压;瑞博生物与齐鲁制药共同开发治疗高血脂症的GalNAc缀合siRNA药物“RBD7022”。
除了心血管疾病外,siRNA药物的龙头企业Alnylam也已经将适应症拓展至血友病、视网膜黄色变性;ASO药物的代表企业Ionis也开展了糖尿病、乙肝病毒感染、前列腺癌的治疗研究。
根据Frost & Sullivan统计,目前全球进入临床的小核酸药物近108个,其中肿瘤已成为小核酸药物临床管线占比最多的适应症,达24%,其余还有遗传病(22%)、感觉器官疾病(13%)、心血管系统 疾病(12%)等。
国外引领、国内追赶
小核酸药物适应症的拓展刺激了市场的增长。据弗若斯特沙利文统计,小核酸药物全球市场规模从2016年0.01亿美元增长至2022年近38亿美元,复合增长率达295%,呈现井喷式发展。
对于前景极大的小核酸药物市场,不少国际医药巨头早早入局。以葛兰素史为例,从2019年开始,葛兰素史分别与Ionis公司合作开发乙型肝炎治疗的ASO药物;2021年,又获得治疗NASH的RNAi疗法 ARO-HSD;在2022年,再次宣布与 Wave Life Sciences 共同推进ASO的开发。
据统计在2021—2022年之间,葛兰素史与Wave、Arrowhead、Ionis 这三家小核酸领域的领军企业均有合作,累计交易总额超过42亿美元。
与此同时,国内医药企业也逐渐开始布局。君实生物于2023年开启了一项ANGPTL3 siRNA药物临床,成为率先探索小核酸药物的创新药企。恒瑞医药也在同年启动了siRNA药物HRS-5635的临床试验。
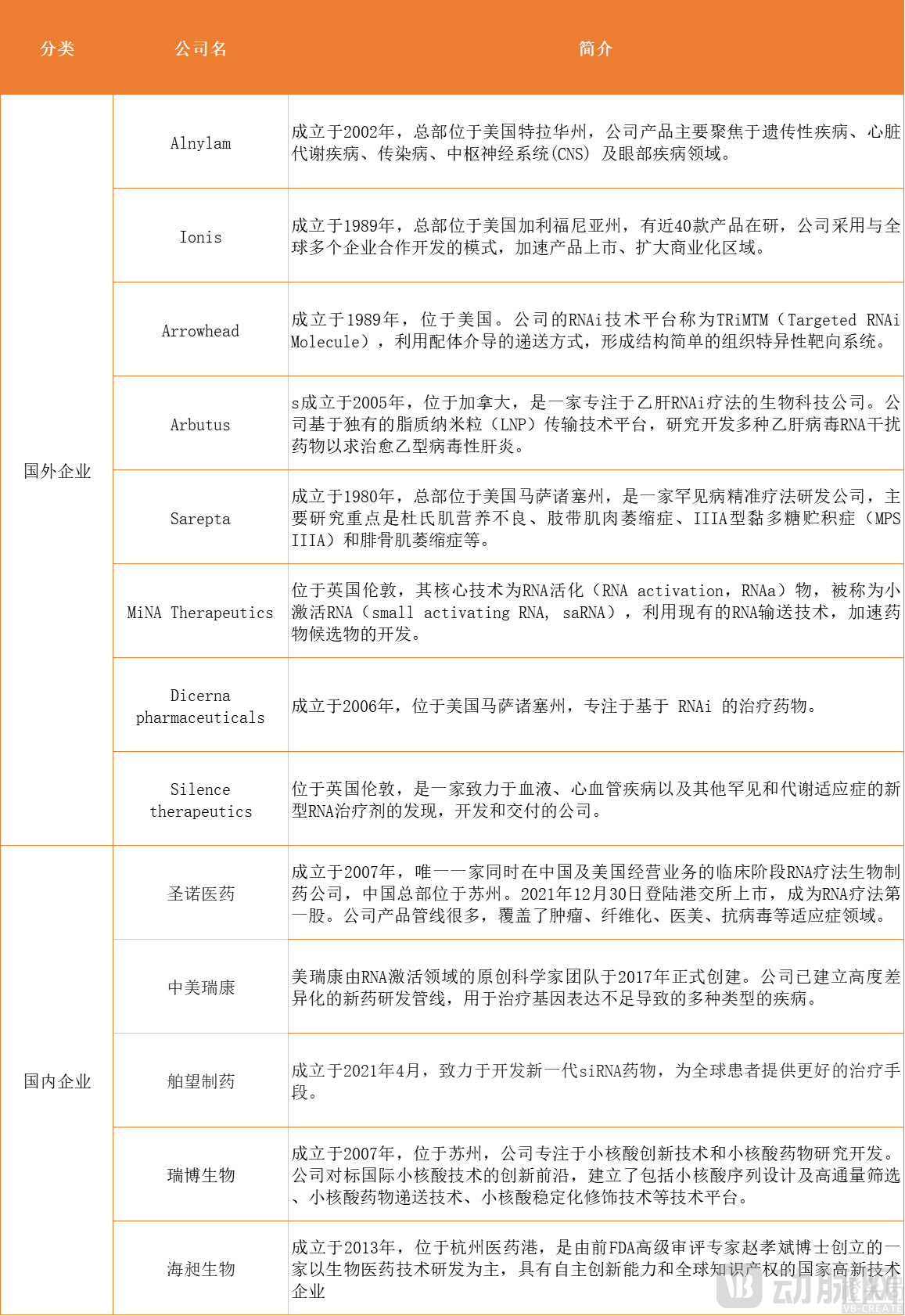
图为国内外部分小核酸药物研发公司
但与国外相比,我国小核酸药物的开发和布局仍处于发展初期。目前,国内仅16款产品处于临床阶段,从产品类型和靶点来看,国内多数企业选择研发的是国外已上市药物的类产品,仍然处于“me-too”阶段。
但随着核心技术的突破,不少国内小核酸创新企业正在加速追赶。据了解,2007年成立的瑞博生物基于其自主研发的GalNAc小核酸药物递送技术平台RIBO-GalSTARTM,已经进入小核酸药物品种的快速开发阶段,拥有8款临床品种。圣诺医药也利用其特色等多肽纳米颗粒(PNP)递送平台GalNAc平台进行小核酸药物研发,正在重点推动STP705治疗皮肤鳞状细胞癌、STP707针对实体瘤、STP122G对抗内源型凝血三个品种等临床研究,产品管线最快的已进入临床Ⅱ期。
不仅如此,“核酸药物发展已经走到转折点”也已经成为学界共识。2023年,在以“核酸生物结构化学与生物医学及健康”香山科学会议学术讨论会上,专家建议建立组织国内科研力量,建立多学科交叉研究的平台,推动核酸药物底层创新研究。这也或将成为推动行业发展和原始创新涌现的关键动力。