
# 热门搜索 #
人工智能辅助新药发现有七个创新方向,可大幅度节省成本和缩短研发时间【2017医疗大数据和人工智能产业报告节选 】
{{detail.short_name}} {{detail.main_page}}
{{detail.description}} {{detail.round_name}} {{detail.state_name}}
 提供支持
提供支持2016 年至今,全世界都在说,人工智能的拐点已来。从世界级的玩家谷歌、IBM,到疯狂的投资人和创业者,都在进行抢点布局,甚至军备竞赛。人工智能正在全球性地走向繁荣。面对如此汹涌而来的人工智能浪潮,我们该如何看待?如何思考?动脉网作为这一浪潮的见证者,势必要为它留下些什么。
动脉网·蛋壳研究院2017年重磅作品——《2017医疗大数据和人工智能产业报告》已于9月16日医疗健康大数据与人工智能产业实践论坛发布。
该报告全文一共10万字, 由蛋壳研究院历时一月,查阅超百万字的资料、采访数10家人工智能公司高层后整理而成。这是动脉网有史以来最为系统地对人工智能医疗领域做出的一次梳理,详细讲述了医疗大数据和人工智能企业的底层技术、医疗人工智能九个细分领域、医疗人工智能企业现状等,并搜集了超过60家国内外企业案例。
获取完整报告的方式:扫描下文二维码,成为动脉网正式会员,即可获得《2017医疗大数据和人工智能产业报告》完整电子版。

以下是报告部分内容的精编连载,实际内容更加丰富。
医疗大数据与人工智能产业报告Ⅳ:药物发现
在药物、生物技术和药理学领域,药物发现是发现新的候选药物的过程。早期,人们只能通过从传统治疗方法或偶然发现鉴定活性成分来发现药物。之后,通过合成小分子、天然产物或提取物在完整的细胞或整个生物体中进行筛选,来鉴定是否是有治疗作用的物质。
新药的开发流程可分为药物发现、临床前开发和临床开发三个部分。而现代药物发现在技术上又可以分为三个阶段:靶点的发现和确证、先导物的发现、先导物的优化三个阶段。
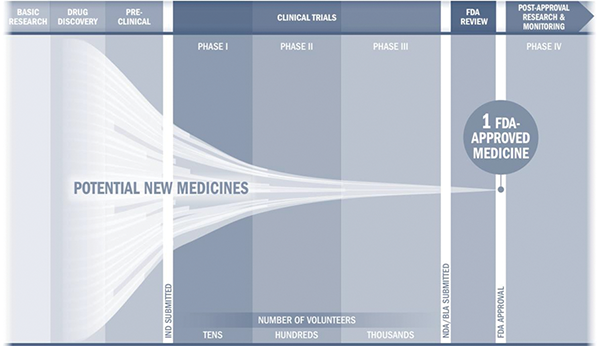
药物发现流程
一、药物发现的现状
药物发现是一种资本密集型的过程,需要药业公司以及各国政府的大量投资。尽管生物技术的不断进步,药物发现仍然是一个昂贵、困难和低效的过程。药物发现的“最终产品”是一个关于潜在药物的专利。之后药物还需要经过非常昂贵的I期,II期和III期临床试验,其中大多数产品会在这过程中被淘汰。
关于创新药研发,国际上有一种“双10”的说法:10年的时间,10亿美金投入。 一般而言,制药公司需要花费5-10亿美金,10到15年时间,才能成功研发出一款新药。新药研发的风险大、周期长、成本高,是药企最大的痛点之一。
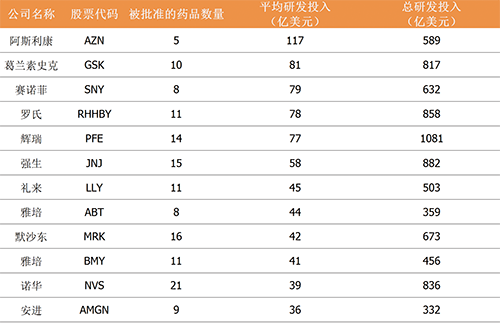
1997年到2011年获批新药研发费用
二、人工智能重构新药研发
目前新药产品的研发越来越难以取得突破。一方面,大多数可以被使用的化合物已经被发现,新的化合物开发难度逐渐加大。另一方面,科学成果的数量增长速度很快,人类个体不可能完全理解这些数据。而人工智能可以从海量论文中摄取所需的分子结构等信息,并且可以自主学习,建立其中的关联,提供新的思路和想法。
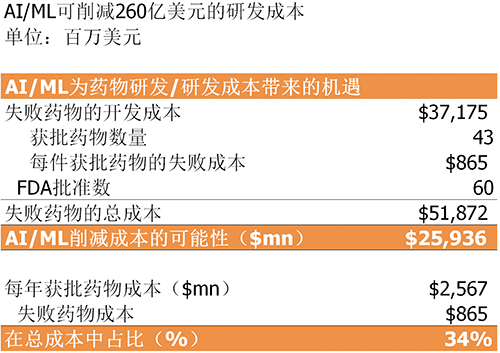
人工智能可以大幅度降低药物研发成本
2015年,FDA报告了60种获批药物。这意味着算上失败药物的研发成本,该年度每种获批药物的的成本约为6.98亿美元,其中就有将近420亿美元用在了失败药物上。蛋壳研究院认为,人工智能可以将新药研发过程中的风险减半:到2025年,全球制药行业每年即可节省约260亿美元。
人工智能的加入,已经开始重构新药研发的流程,人工智能在新药研发上的应用也开始从靶点筛选向更多方面拓展。
根据在流程上的分布,我们将AI+新药研发的服务类型分成了三类:临床前药物发现服务、临床前药物自主研发和临床研究服务。 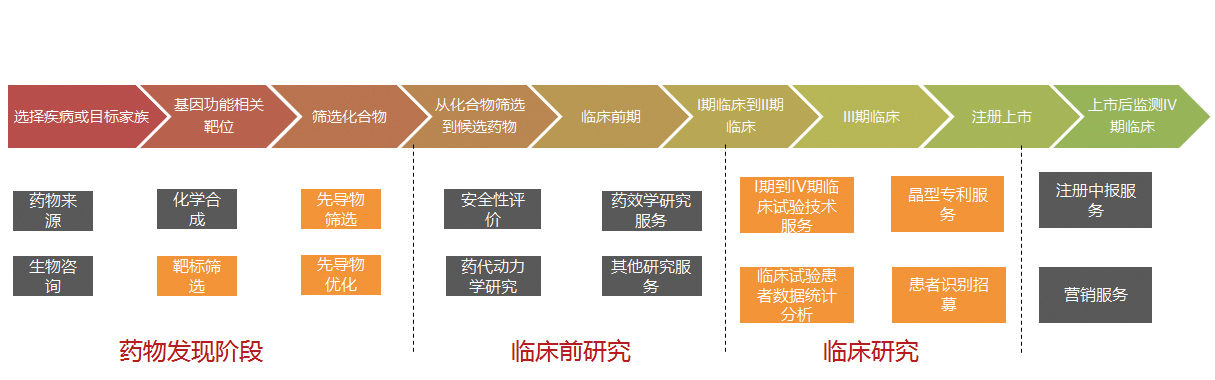
人工智能参与药物研发的方式
三、制药企业纷纷布局
一直观望AI发展的制药公司现在纷纷涉足AI领域。
Numerate公司与武田药业(Takeda Pharmaceutical)正式签约,就使用Numerate公司的人工智能技术(artificial intelligence, AI)寻找肿瘤学、胃肠病学和中枢神经系统疾病的小分子药物展开合作。
葛兰素史克公司(GSK)与Exscientia达成合作。这笔交易涉及金额约为4300万美元。双方合作之后,Exscientia将利用其AI药物研发平台为GSK进行10个创新小分子药物疾病的靶点开发。
包括默克(Merck & Co)、强生(Johnson & Johnson)和赛诺菲(Sanofi)在内的其他制药巨头也在探索人工智能的潜力,以帮助简化药物研发过程。

制药企业和人工智能新药研发企业进行合作开发
四、人工智能+新药研发的七个创新方向
人工智能在新药研发上的应用主要可以是两个阶段:一个是新药发现阶段,另一个是临床试验阶段,共七种不同应用方向。

各个新药研发阶段的人工智能新药研发企业
1.靶点筛选
靶点发现也就是发现能减慢或逆转人类疾病的生物途径和蛋白,这是目前新药发现的核心瓶颈。针对前沿论文分析和处理并提供预测数据我们也可以看作在靶点筛选上的应用。老药新用是目前寻找药物的常用方式,他的实现方式是将市面上已曝光的药物及人身上的1 万多个靶点进行了交叉研究及匹配。以往这项工作由人工试验完成,现在通过人工智能参与,将给试验的速度带来指数级的提升。据推测,搭建算法模型及大规模的算力,利用“老药新用”这一手段手段有望将药物研发成本降至3亿美元甚至更低,研发周期也缩短至6.5年。
在科学研究飞速发展的今天,每30秒就会有一篇生命科学论文发表。除此以外,还有大量的专利、临床试验结果等海量信息散布在世界各地。这些信息中,只有一小部分的科学信息可以形成有用的新知识。对于药物研发工作者来说,他们没有时间和精力来关注所有的新信息,但是这些信息又包含了全球大部分科研人员的研究成果和大量关于新药的信息,从这些信息中找寻新药的蛛丝马迹是药物发现的一种捷径。
2.药物筛选
药物筛选,也可以称为先导物筛选。制药企业积累了大量调控蛋白功能的小分子化合物,大规模的跨国药企一般都会有50-300万的化合物储备。先导物发现首先通过少数模块组合成不同蛋白,然后会采用高通量筛选来发现合适的先导物。高通量筛选方式会在同一时间由机器人进行数以百万计的试验,因此成本非常高昂。迄今为止,学者们已经纷纷倡导利用AI/ML开发有效和准确的虚拟筛选方法,以取代昂贵且耗时的高通量筛选过程。
现有虚拟筛选的方法名为“高通量筛选”,而它非常容易受到FDR(错误发现率)的影响。如果可以将第3阶段试验的风险减半,就可以为大型制药公司节约数十亿美元的成本,
针对药物筛选阶段,人工智能有两种应用方案,一种是利用深度学习开发虚拟筛选技术以取代高通量筛选,另一种是利用人工智能图像识别技术优化高通量筛选过程。
谷歌和斯坦福的研究人员正致力于利用深度学习开发虚拟筛选技术,以取代或增强传统的高通量筛选过程,并提高筛选的速度和成功率。通过应用深度学习,研究人员能够实现跨越多个靶点的众多实验的信息共享。正如Bharath Ramsundar 等在其一篇机器学习相关的论文中所称:“我们的实验表明,深层神经网络优于所有其他方法……尤其在于,深层神经网络大大超越了所有现有的商业解决方案。在许多靶点上,它都实现了接近完美的预测质量,使其尤其适合被用作虚拟筛选装置。总之,深度学习提供了建立虚拟筛选并将其作为药物设计管道中标准步骤的机会。”(Massively Multitask Networks for Drug Discovery,2015/2/6)
3.药物优化
药物优化又可以叫做先导物优化,这个步骤主要是对先导物的构效关系进行优化。这个阶段需要全面改进先导物的分子缺陷,当代药物发现有时可能有20~30个指标需要同时优化,而分子改造牵一发而动全身。借助人工智能,能够以直观的方式定性推测生理活性物质结构与活性的关系,进而推测靶酶活性位点的结构和设计新的活性物质结构。可以进一步提升药物的构效关系分析的速度,快速挑选最具安全性的化合物。
4.病人识别及招募
招募合适的志愿者一直是制药公司面临的难题之一,在时间就是金钱的药物研发过程中,除了招募的直接成本,由于延长时间造成的间接成本也不容忽视。在实际过程中,大多数临床试验不得不大幅延长其时间表,因为在原定时间内很难发现足够数量的患者。这类麻烦并不罕见,根据拜耳的数据,90%的临床试验未能在指定时间内招募到足够数量的患者,通常而言所耗费的时间是指定时间的两倍左右。利用人工智能对疾病数据深度研究,制药企业可以更精准挖掘目标患者,快速实现患者招募。
2016年,Biogen进行了一项研究,使用Fitbit追踪多发性硬化症患者的活动。结果,24小时内便成功招募了248名患者,其中77%的人完成了后续研究。这项实验显示,有一小部分可穿戴设备使用者非常愿意自我量化,并分享他们的生理数据。使用数字健康设备(包括医疗级的可穿戴设备)招聘大量的志愿者参加临床试验正在成为趋势。
5.服药依从性管理
依从性是指病人执行医嘱的客观应答的程度。在新药临床试验中,依从性可定义为受试者按照规定的药物剂量和疗程服用试验药物的程度。传统方式服药依从性主要通过人工随访来管理,如果数据量大则只能依靠病人的自觉性。在这个阶段我们利用移动技术和面部识别技术来判断患者是否按时服药,用自动算法来识别药物和药物摄取,并且可以提醒患者按时服药,对患者的服药依从性做出精准管理。
6.患者数据收集
在传统的新药研发流程中患者的健康状况和身体数据情况只能在临床中进行评估,病人需要进行定期检查,特定时间和地点获得的数据并不能完整的代表病人的身体情况,容易出现数据偏差。在这个阶段可以应用可穿戴设备与机器学习分析来提升临床试验中的患者参与度、数据质量和操作效率。
生命科学临床研究领域云解决方案供应商Medidata宣布与Garmin达成战略合作,通过Garmin的健康手环与MedidataClinicalCloud相结合的方式提升临床试验中的患者参与度、数据质量和操作效率。此外,VitalConnect等公司还获得了FDA的批准,利用其生物传感器来监测患者的各项生物指标。这些生命科学公司正把我们推向一个新的时代,连接到之前根本无无法获取的一系列新行为数据。前文所述案例均能让我们在临床试验中提升患者互动,最终让我们获得更多、更实用的数据,这些对于药物研发取得突破至关重要。
7.小分子药物晶型预测
药物晶型对于制药企业十分重要,其不但决定小分子药物的临床效果,同时具有巨大的专利价值。药物晶型专利是药品化合物专利之后的最重要的专利,是原研药企业阻止或推迟仿制药企业在其化合物专利过期后将仿制药推入市场的重要筹码,药物晶型专利可以延长药物专利2 到6 年,对于重磅药物而言,则意味着数十亿美元的市场价值。
利用人工智能,高效地动态配置药物晶型,可以把一个小分子药物的所有可能的晶型全部预测。相比传统药物晶型研发,制药企业无需担心由于实验搜索空间有限而漏掉重要晶型,可以更加自如地应对来自仿制药企的晶型专利挑战。此外,晶型预测技术也大大缩短了晶型开发的周期,更有效地挑选出合适的药物晶型,缩短研发周期,减少成本。
如果您想对接动脉网所报道的企业,请填写表单,我们的工作人员将尽快为您服务。